El cloro y sus compuestos es un desinfectante de uso mayoritario por ser un excelente bactericida muy económico y de fácil aplicación.
En estado gaseoso es de color amarillo verdoso, líquido es amarillo y el sólido es de color ámbar, no se encuentra en la naturaleza como elemento químico, siempre aparece combinado con otros elementos, principalmente como sal común, en algunos sólidos o en el agua.
En la actualidad su uso principal es como materia prima en los plásticos, productos de limpieza, muebles, papel, herbicidas, insecticidas, entre otros productos. Por otro lado, también se usa en la producción de otros productos químicos.
Con respecto a tratamiento de aguas, los compuestos basados en cloro son los únicos desinfectantes importantes que presentan propiedades residuales duraderas.
La protección residual impide un nuevo crecimiento microbiano y previene la contaminación del agua hasta su uso por el destinatario.
La cloración del agua potable reduce los gustos y olores, el cloro oxida muchas sustancias que se presentan naturalmente, tales como las secreciones de algas malolientes y los olores de la vegetación en descomposición, lo que da como resultado agua potable inodora y con mejor sabor.
El efecto desinfectante se debe a la oxidación de la materia orgánica viva (microorganismos), materia orgánica muerta e incluso sobre ciertos compuestos minerales.
 Para entender el comportamiento del cloro en el agua hay dos aspectos fundamentales que tenemos que conocer:
Para entender el comportamiento del cloro en el agua hay dos aspectos fundamentales que tenemos que conocer:
-
La influencia del pH del agua en la eficacia de la desinfección del cloro.
-
Cómo se comporta el cloro en medio acuoso frente a la materia orgánica.
1. La influencia del pH del agua en la eficacia de la desinfección del cloro.
El cloro es soluble en agua a temperatura ambiente (20º) puede estar en otras formas, tales como ácido hipocloroso (HOCl) o ion hipoclorito (OCl– ) cuya relación depende del pH del agua. La eficiencia germicida del ácido hipocloroso (HOCl) es de 60 a 100 veces más eficaz la del ión hipoclorito (OCI–).
El rango de pH donde el cloro es eficaz como germicida está entre 7.2 y 7.6
Para garantizar la desinfección con cloro es imprescindible disponer de un control sobre el valor del pH
Veamos la razón:
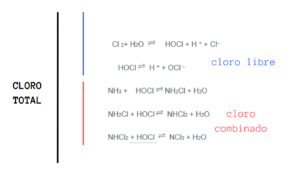
Cl 2+ H2O ⇔ HOCl + H + + Cl–
HOCl ⇔ H + + OCl – Cuando el valor del pH del agua varía, el equilibrio de esta reacción se modifica y con ello la capacidad de desinfección del cloro
Cuando bajamos el pH en el agua a valores cercanos a 7.2 aumenta la concentración de iones H + que se unen al ión Hipoclorito (OCl–) el equilibrio se desplaza hacia la izquierda para crear el ácido hipocloroso (HOCl) La capacidad de desinfección aumenta
Si el pH aumenta, disminuye la concentración de H + el equilibrio se desplaza a la derecha, por lo que el HOCL de disocia para crear el OCl– y H + La capacidad de desinfección disminuye
Y fuera de este rango ya el cloro pierde su eficacia como germicida
2-Cómo se comporta el cloro en medio acuoso frente a la materia orgánica.
Es importante saber cómo se comporta el cloro ante los compuestos y elementos que se va a encontrar en el agua, para poder calcular cuánto cloro deberemos adicionar para su tratamiento.
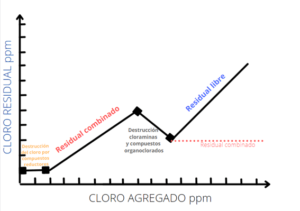
En un primer momento no todo el cloro que estamos aportando al agua, está desinfectando, parte del cloro se invierte en reaccionar con la materia orgánica y en oxidar sustancias inorgánicas reductoras. Así pues, hasta que no sucedan estas primeras reacciones, no tendremos una relación lineal, entre el cloro adicionado y el cloro activo (que desinfecta), a estos les llamamos; cloro residual total y cloro residual libre.
La cantidad de cloro que tenemos que adicionar para tratamiento de agua va a depender de la materia orgánica que esta contenga.
Veamos paso a paso cómo sucede:
-
- Lo primero que hace el cloro es oxidar sustancias inorgánicas, fundamentalmente compuestos reducidos de hierro, manganeso y azufre y los nitritos.
- Después reacciona formando compuestos orgánicos de cloro y cloraminas a este cloro se le llama cloro residual combinado.
- Finalmente llega un momento que se produce la oxidación completa de los compuestos organoclorados y de las cloraminas, por lo que ya no es detectable en el agua el cloro residual combinado.
- Si el cloro residual total= cloro residual libre + cloro residual combinado A partir de este momento la relación entre el cloro libre y el cloro total comienza a ser lineal.
Si analizamos ambos podemos saber en qué momento del proceso se encuentra el agua a tratar.
Por tanto, cuando medimos con un analizador de cloro tenemos que saber cuál de las dos concentraciones de cloro estamos midiendo.
Puedes entrar en la nuestra tienda online para ver los analizadores de cloro y si tienes dudas ponte en contacto con nosotros.
Puede ser con reactivos líquidos o con pastillas
enlace a la tienda online :
#Hipoclorito #Cloro
Estamos en:
HORARIO DE VERANO:
L-V continuado 09:00 a 19:00 horas
Los sábados 09:00 a 14:00 horas
HORARIO DE INVIERNO:
L-V Mañana 09:00 a 14:00 horas
Tarde: 16:00 a 18:00 horas.
«Tienda Los Abuelos»
🏠Calle Plomo, 8 Polígono de San Cristóbal
📲983 232 336 llámanos para cualquier consulta
🌐 www.losabuelos.es
📩info@losabuelos.es
Fuentes:
- Química inorgánica Catherine E. Housecroft, Alan G. Sharpe
- Trabajo de fin de máster módulo de química inorgánica e ingeniería química el cloro, producción e industria autor/a: Lucía Noval Gómez Disponible en cloro trabajo fin curso.pdf
- Blog https://purewater.com.co/quimica-basica-del-cloro/
- Universidad de Salamanca CLORACION (CLOROMETRIA) (usal.es)